Un guide de poche sur les conformités en matière de soins de santé
Publié: 2020-06-26La santé est l'un des secteurs dominants qui est bombardé de technologies numériques dans le but de moderniser son paysage infrastructurel et ses services.
Si l'on prend les dépenses institutionnelles comme référence, les soins de santé dépassent de loin les dépenses du gouvernement américain, en correspondance avec d'autres secteurs. En 2017, les États-Unis ont alloué 3,5 billions de dollars aux soins de santé. En pourcentage du PIB du pays, cela s'élevait à 17,7 % . La santé, aux États-Unis, n'est pas un territoire confiné aux entreprises héritées avec des chargements de capitaux à investir et à développer, mais ouvert à tous pour la participation.
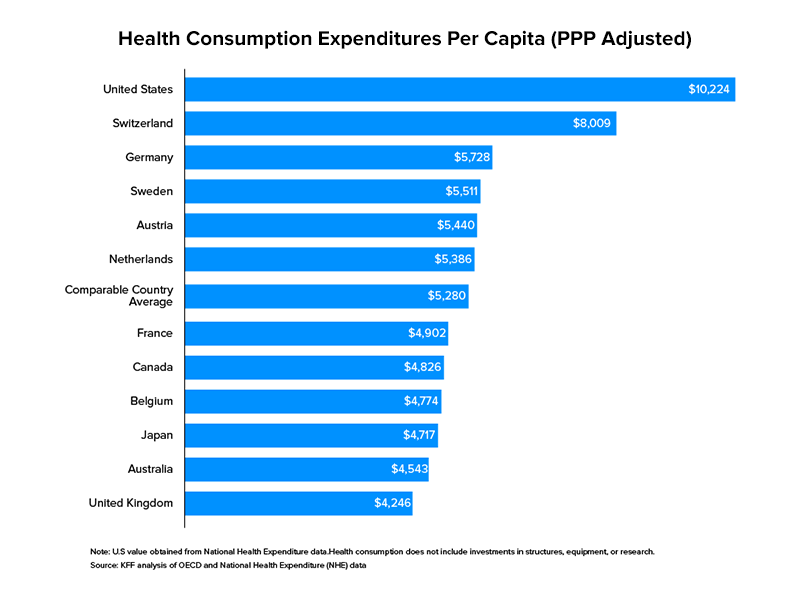
La santé numérique est une perspective en développement de cette industrie qui englobe des modèles commerciaux tels que la télésanté, la surveillance à distance via des applications pour smartphone et la livraison à domicile de médicaments sur ordonnance. Rien qu'en 2019, plus de 17 milliards de dollars ont été levés par des startups prônant l'adoption des soins de santé numériques dans plus de 1 700 transactions aux États-Unis. Comme prévu dans ce changement en cours, le développement des soins de santé mobiles occupe le devant de la scène.
Développer un produit qui prétend avoir un impact/améliorer l'hygiène personnelle est un problème difficile à résoudre, non pas à cause des défis des services de développement de logiciels de santé impliqués, mais à cause des directives fiduciaires.
Appinventiv est à la pointe de ce changement qui fait battre le cœur de l'industrie grâce à ses partenaires. En tant qu'entreprise de développement d'applications de soins de santé , nous sommes passés par là et nous l'avons fait, ce qui était nécessaire pour concrétiser des idées novatrices . En tant que votre confident, nous discuterons aujourd'hui des réglementations et de la conformité communes que vous devez garder à l'esprit lors du développement d'une application mHealth .
Qu'est-ce que la conformité à la réglementation des soins de santé ?
La conformité réglementaire dans le domaine de la santé concerne l'adhésion d'une association médicale aux lois, directives, réglementations et spécifications applicables à ses processus commerciaux. La violation de la conformité réglementaire entraîne régulièrement des sanctions légales, y compris des amendes fédérales. Il s'agit du cycle continu de respect ou de dépassement des normes légales, morales et professionnelles applicables à une association ou à un fournisseur de soins de santé spécifique.
Actuellement, les entreprises de soins de santé comme les hôpitaux et les prestataires de soins de santé ont des membres d'équipe dédiés qui se concentrent spécialement sur la conformité réglementaire. La raison et l'avantage essentiel des exigences réglementaires pour les hôpitaux sont d'améliorer les soins aux patients.
Quel est le but de la conformité dans les soins de santé ?
La conformité des soins de santé est un segment fondamental de chaque fournisseur de soins médicaux. C'est la façon de suivre les règles, les lignes directrices, les lois et les règlements liés à la pratique des services de santé.
La conformité dans les soins de santé couvre un large éventail de pratiques et observe des règles internes et externes. Cependant, la plupart des problèmes de conformité des services médicaux s'identifient à la sécurité des patients, à la protection des données des patients et aux répétitions de facturation.
La branche américaine de la santé et des services sociaux (HHS) a établi des normes nationales connues sous le nom de Health Insurance Portability and Accountability Act (HIPAA), et la caractéristique centrale de la conformité médicale est de faire respecter cette législation.
Pourquoi la conformité des soins de santé est-elle importante ?
La conformité assure le bon déroulement des tâches et garantit que tout le monde suit les procédures légitimes et comprend les hypothèses.
Pourtant, la conformité dans les services médicaux s'accompagne d'enjeux nettement plus élevés que dans d'autres secteurs. D'un autre côté, si les médecins comme les médecins et les infirmières ne suivent pas la procédure légitime, ils peuvent finir par nuire à un patient ou à un autre membre du personnel.
En fin de compte, la conformité aux soins de santé consiste à fournir des soins aux patients sûrs et de haute qualité. Le respect des normes et réglementations de l'industrie aide les organisations de soins de santé à continuer d'améliorer la qualité des soins.
Enfin, la conformité des soins médicaux consiste à prodiguer des soins protégés, de qualité et sûrs aux patients. Le respect des directives et des réglementations de l'industrie aide les organisations de soins de santé à continuer d'améliorer la qualité des soins.
Les organisations de soins de santé sont tenues de respecter des directives, des lois et des réglementations strictes du gouvernement. Les violations de ces lois peuvent entraîner des poursuites, de lourdes amendes ou même la perte de licences.
Qu'est-ce qu'un risque élevé de problèmes de conformité ?
Un cadre réglementaire sert de modèle utilisé pour sanctionner les lignes directrices. De telles structures pourraient être créées dans des domaines d'intérêt explicites, comme l'industrie de la santé. Les gouvernements dépendent fréquemment de l'utilisation de ces cadres pour créer et promulguer des directives, des règles et des lois. Les cadres réglementaires sont généralement d'abord élaborés en tenant compte de l'objectif final.
Examinons la principale question qui préoccupe tout le monde, c'est-à-dire quels sont les problèmes de conformité dans les soins de santé ?
HIPAA et violations de données
Ententes de rémunération fondées sur la valeur
Problèmes anti-recul et médecin-hôpital
Processus de diligence raisonnable
Qualifications des fournisseurs de télésanté
Entrepreneurs en audit de recouvrement
Hôpitaux exonérés d'impôt et exigences de conformité
Réglementation et conformité des soins de santé aux États-Unis
La santé numérique a des restrictions détaillées indiquant les choses à faire et à ne pas faire pour les technologies de l'information sur la santé (HIT), la santé mobile, les prescriptions personnalisées, la technologie portable et la télésanté. Les applications mobiles sont l'un des moyens les plus courants de prestation de soins de santé , que ce soit par le biais d'un service hors ligne ou en ligne ou d'un logiciel en tant que service. Si tel est le cas, les entrepreneurs doivent se poser les questions suivantes et y trouver des réponses objectives :

Le questionnaire ci-dessus délimitera si votre application mobile nécessite ou non une autorisation fiduciaire. Si vos réponses étaient majoritairement oui, trois organismes fédéraux se pencheront sur la question de votre produit mHealth :
- Administration des aliments et des médicaments (FDA)
- Commission fédérale du commerce (FTC)
- Bureau des droits civils (OCR)
Ci-dessous, nous examinons les principaux domaines de fonction fédéraux et la portée de la vérification granulaire des faits sur lesquels une société de développement de logiciels de santé doit conseiller ses clients.
1. Loi sur la portabilité et la responsabilité de l'assurance maladie (HIPAA)
Cette loi est appliquée par l'Office for Civil Rights (OCR) au sein du Département américain de la santé et des services sociaux. Cette règle de sécurité HIPAA conforme aux normes médicales protège les préoccupations de confidentialité et de sécurité des données éligibles liées à la santé et, dans des cas particuliers, rend obligatoire le signalement des violations de données. Le non-respect d'une règle de sécurité particulière de la HIPAA pourrait entraîner des sanctions à partir d'un paiement minimum de 100 $ et pouvant atteindre 1,5 million de dollars par incident.
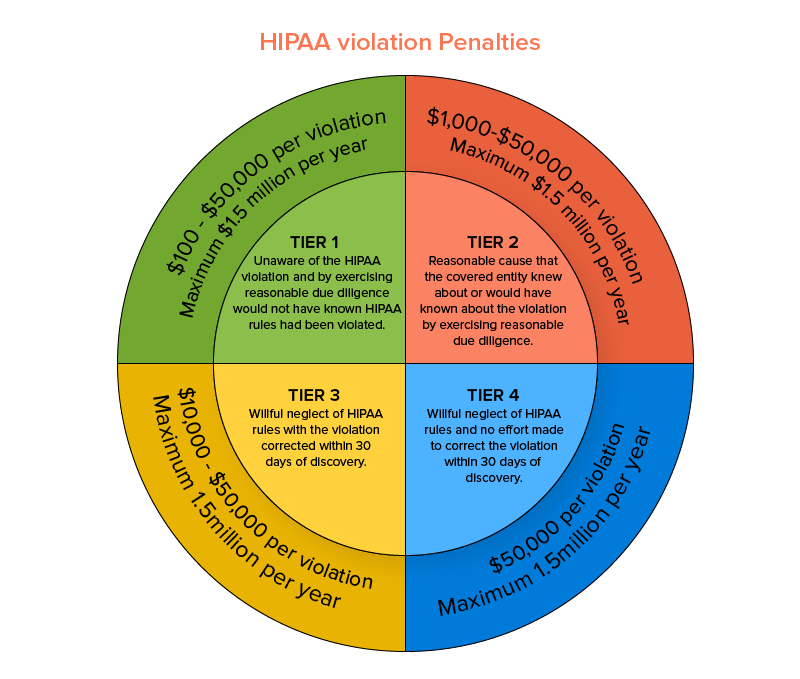
Maintenant que vous avez une idée palpable du sérieux avec lequel aborder l' exigence de la réglementation des soins de santé , nous devrions continuer et examiner les types d'applications médicales qui devraient se conformer aux politiques traditionnelles de HIPAA. Trois 3 facteurs régissent les critères d'éligibilité définis pour qu'une application soit distinguée comme médicale en termes opérationnels :
I. La nature de l'entité qui utilise l'application.
L'entité fait référence au client qui utiliserait l'application. Il existe un ensemble de médecins prédéfinis qui sont couverts par la constitution de la HIPAA, tels que les médecins, les médecins, les organisations telles que les hôpitaux et les prestataires d'assurance maladie. S'ils sont les bénéficiaires directs de l'application, la liste des réglementations en matière de soins de santé et la conformité réglementaire des hôpitaux par HIPAA devront être suivies mot pour mot. D'un autre côté, si l'application se contente de conserver et de partager des conseils d'hygiène ou des connaissances sur le bien-être avec le client, cela sera exempté de la constitution de HIPAA.
II. La nature des données que l'application produit, conserve et partage davantage.
Les données sont essentielles aux besoins de fonctionnement des entreprises en ligne. Les autorités fédérales font pression pour des lois qui annulent les problèmes de sécurité tels que les violations de données et garantissent la présence d'une infrastructure de cryptage robuste. Essentiellement, les données collectées ne doivent pas et ne doivent pas conduire des acteurs malveillants vers des personnes via leurs informations personnelles telles qu'une adresse, un numéro de sécurité sociale, etc. Si l'application traite de l'utilisation de tels points personnels, alors les règles HIPAA s'appliquera.

III. Le logiciel sous-jacent qui alimente l'application.
Le meilleur développement d'applications mobiles de soins de santé doit se concentrer sur l'innovation d'une application téléphonique sécurisée. HIPAA partage les détails des informations de santé protégées (PHI) et ordonne aux éditeurs de logiciels de créer un filet de sécurité autour d'eux. Ses directives ont une liste de contrôle approfondie des audits et des contrôles internes à installer pour PHI.
2. Loi sur la commission fédérale du commerce (loi FTC)
Cette loi impose des protocoles réglementaires pour traiter les réclamations injustes et les pratiques abusives dans les entreprises, également liées aux questions de confidentialité et aux défis généraux de sécurité des données. Les réclamations non fondées concernant l'utilisation d'une application sont couvertes par cette loi. La règle de notification des violations de la santé de la FTC oblige certaines entreprises à signaler les violations de données telles que les dossiers de santé personnels.
3. Loi fédérale sur les aliments, les médicaments et les cosmétiques (FD&C Act)
La Food and Drug Administration est chargée de mettre en œuvre cette loi. Leur objectif premier est de s'assurer que les dispositifs médicaux, y compris les applications mobiles, répondent aux directives standard et peuvent donc être consommés en masse en toute sécurité. Il est primordial que nous mentionnions que toutes les applications de soins de santé ne relèvent pas de cette juridiction, mais quelques-unes. Ce sont ceux qui, s'ils ne répondent pas aux exigences, entraînent de graves conséquences pour la santé des consommateurs.
Règlement additionnel Pour la santé numérique
Alors que les actes ci-dessus étaient des applications de soins de santé incisivement ciblées, il y en a d'autres qui n'ont pas été instituées pour la raison mais ajustées pour inclure la même chose. Dans cette section, nous allons évaluer un aperçu de ces normes soutenues par l'État auxquelles les entrepreneurs mHealth doivent adhérer.
1. Administration des aliments et médicaments (FDA)
La Food and Drug Administration est une agence soutenue par le gouvernement américain qui constitue un élément clé du département américain de la Santé et des Services sociaux. Les développeurs d'applications de soins de santé doivent tenir compte d'un tel ensemble de directives bien définies lors de la conception d'applications pour obtenir une autorisation de la FDA. Pour le secteur de la santé numérique, la FDA catégorise les applications mobiles en dalles « médicales » sur la base des deux postulats suivants :

- L'application est utilisée comme accessoire avec ou avec un dispositif médical déjà réglementé.
- L'application transforme la plate-forme mobile en un appareil mobile réglementé
Sur la base de la classification de premier niveau susmentionnée, le sous-secteur de l'application est défini en fonction de sa relation avec les technologies numériques émergentes suivantes pour se rapprocher d'une approbation de la FDA.
I. Logiciel en tant que dispositif médical (SaMD)
SaMD est défini comme un modèle où le logiciel est utilisé à des fins médicales sans être associé à un instrument/dispositif médical matériel. Le modèle est très flexible et peut être appliqué à une gamme de plates-formes allant des réseaux virtuels aux dispositifs médicaux.
Le Forum international des régulateurs des dispositifs médicaux (IMDRF) est une coalition mondiale qui prône une gouvernance systématique des dispositifs médicaux. En 2013, il a formulé le groupe de travail sur les logiciels en tant que dispositifs médicaux (SaMDWG) afin d'introduire des conseils pratiques pour soutenir l'avancement des technologies numériques dans ce segment. Dirigé par la FDA elle-même, le groupe a documenté une pléthore de cadres sur :
- Définitions
- Catégorisation des risques
- Système de gestion de la qualité
- Évaluation clinique
Parcourir leurs catalogues vous aidera à déterminer si vous obtiendrez ou non une approbation SaMD.
II. Dispositifs médicaux sans fil
Il fait référence à des dispositifs médicaux équipés de la capacité d'effectuer une transmission sans fil de données d'information pour faciliter les services de soins de santé. Ces boîtes à outils déploient des fréquences radio pour la communication qui peuvent être transmises via WiFi, Bluetooth ou un smartphone. Un exemple courant, que vous avez peut-être trouvé dans les bureaux de l'entreprise, est celui des dispositifs d'identification par radiofréquence (RFID).

III. Télémédecine
L'informatique de santé est divisée en télémédecine et télésanté afin de simplifier le processus d'obtention de l'approbation de la FDA. La télésanté est désignée comme l'utilisation des télécommunications pour promouvoir et soutenir les fonctions liées aux soins de santé - une fonction qui est d'autant plus sous les feux de la rampe depuis l'épidémie de COVID-19 . Une société de développement de logiciels de soins de santé personnalisés pourrait développer des applications qui utilisent :
- Visioconférence en direct (asynchrone)
- Vidéoconférence avec stockage et retransmission (asynchrone)
- Surveillance à distance des patients (RPM)
- Santé mobile (mHealth)
IV. Informatique de santé
Dans ce cas, nous ferions mieux de citer la définition fournie par le bureau du gouvernement fédéral du coordinateur national des technologies de l'information sur la santé, "matériel, logiciel, technologies intégrées ou licences connexes, propriété intellectuelle, mises à niveau ou solutions packagées vendues en tant que services qui sont conçus pour ou soutiennent l'utilisation par des entités de soins de santé ou des patients pour la création, la maintenance, l'accès ou l'échange électroniques d'informations sur la santé.
V. Systèmes de données sur les dispositifs médicaux (MDDS)
Les produits matériels/logiciels qui peuvent être utilisés pour canaliser des données, conserver/stocker des informations, convertir des données d'un format à un autre ou simplement afficher des données scientifiques/médicales relèvent de la catégorie MDDS. L'objectif de tels dispositifs n'est pas d'apporter des caractéristiques supplémentaires ou d'enrichir le jeu de données mais simplement de l'afficher.
VI. Interopérabilité des dispositifs médicaux (MDI)
Il n'y a sans doute aucun autre sous-domaine de la santé numérique où le concept d'une application téléphonique sécurisée augure parfaitement bien que MDI. L'interopérabilité des dispositifs médicaux fait référence à l'échange interplateforme/technologique d'informations entre plusieurs dispositifs. Contrairement à MDDS, où le motif principal est la présentation, les applications MDI peuvent afficher, stocker et analyser des données. Grâce à la communication aller-retour, ils peuvent également être utilisés pour contrôler d'autres produits.
VII. Fonctions du logiciel de l'appareil
Lorsque l'on parle de cette catégorie, l'autorisation n'est accordée qu'aux applications logicielles qualifiées d'« appareils » selon les directives de la FDA. Les dispositifs logiciels qui présentent un risque minimal ou nul pour la consommation peuvent ne pas nécessiter une approbation officielle de la FDA et l'organisation est explicite lorsqu'elle dit que dans de tels cas, il
» exercera son pouvoir discrétionnaire d'application et ne s'attendra pas à ce que les fabricants soumettent des demandes d'examen préalable à la commercialisation ou qu'ils enregistrent et répertorient leurs logiciels auprès de la FDA. ”
VIII. La cyber-sécurité
La cybersécurité en soi n'est pas un mode de classification pour une application mHealth. Pourtant, la FDA souhaite établir un protocole d'accord clair afin de pouvoir peser les défis de sécurité des données que pose l'application par rapport aux avantages pour les utilisateurs.
IX. Intelligence artificielle/Apprentissage automatique
L'impact de l'IA sur les soins de santé est disproportionnellement gargantuesque par rapport aux autres technologies. Pourtant, les progrès dans ce secteur sont plutôt récents, ce qui a obligé la FDA à apporter des ajustements à ses cadres réglementaires. Conformément à ses dernières directives, la FDA travaillera main dans la main avec les fabricants pour évaluer en permanence le logiciel à partir de ses étapes de développement pré-commercialisation et culminant à l'étape de performance post-commercialisation. Le cadre s'applique spécifiquement à SaMD.
2. Normes HL7
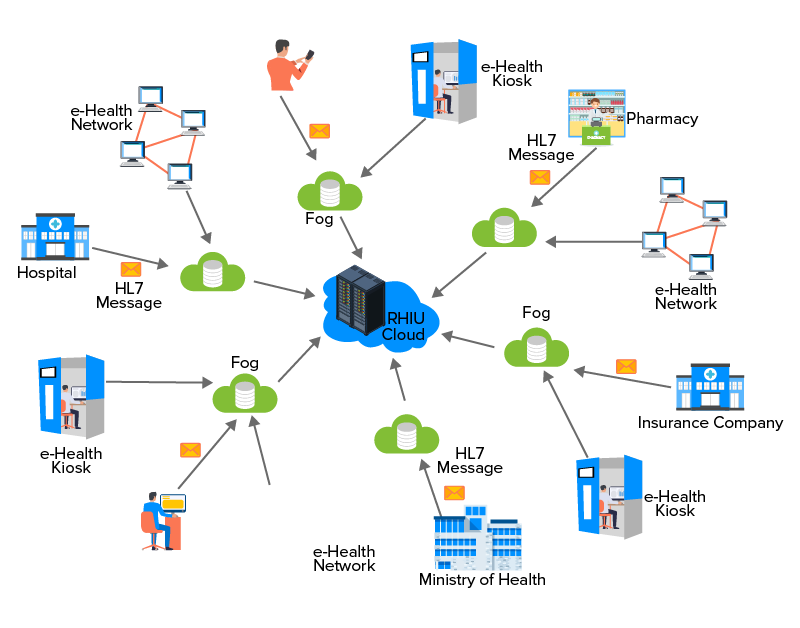
Health Level Seven International, simplement appelé HL7, est une organisation à but non lucratif constituée en 1983 qui développe des références de l'industrie pour l'échange, l'intégration, le partage et la récupération d'informations de santé électroniques qui permettent la pratique médicale procédurale. En plus de cela, les normes HL7 jouent un rôle rudimentaire dans la gestion des services de santé, en gardant le cap pour une prestation de soins de santé transparente et en évaluant les résultats.
Comment font-ils cela?
Les normes HL7 définissent le conditionnement des informations pour qu'il soit interopérable entre deux applications de soins de santé, dictant le flux de travail pour la langue, les formats de données et sa structure afin de s'intégrer facilement dans les systèmes. Ce faisant, ils réduisent les investissements dans les infrastructures technologiques et profitent aux patients, rendant ainsi les soins de santé plus abordables. Se conformer aux règles rédigées afin d'obtenir une approbation HL7 comporte un double avantage pour la réglementation de l'industrie de la santé . D'abord, l'application de soins de santé est universellement acceptée et prête à être déployée dans le monde entier. Et deuxièmement, le coût de développement d'applications est réduit.
3. La loi HITECH
La loi sur les technologies de l'information sur la santé pour la santé économique et clinique a été introduite sous le régime du président Barack Obama en 2009. L'objectif de la loi HITECH était de promouvoir l'adoption par les entreprises des technologies de l'information sur la santé par le biais des dossiers de santé électroniques (DSE). L'administration a également resserré les détails autour de la loi HIPAA de 1996, à la suite de laquelle il est devenu obligatoire pour les entreprises de soins de santé d'informer les clients si et quand leurs informations d'identification ont été compromises.
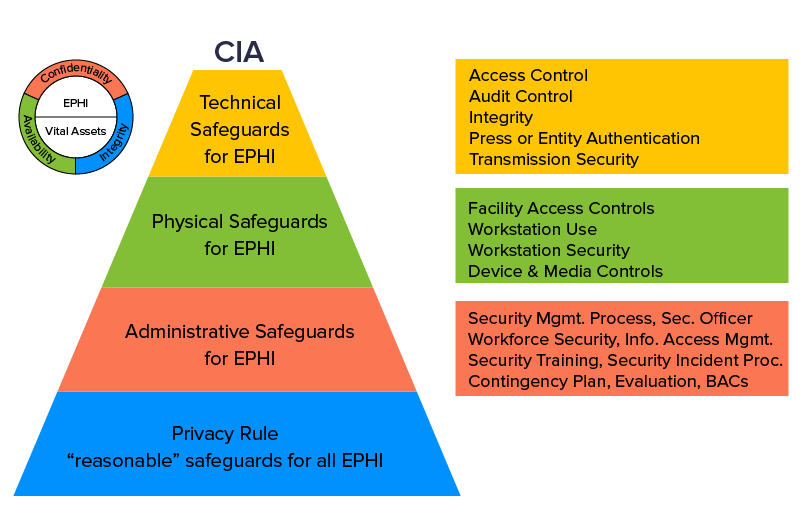
L'effet immédiat de la loi HITECH a été que le partage d'informations entre deux entités distinctes est devenu plus facile à gérer grâce aux DSE. La loi garantissait également l'installation d'une infrastructure de sécurité difficile à atteindre en cohérence avec les impératifs de confidentialité et de sécurité de la loi HIPAA. Toutes les exigences réglementaires pour obtenir une approbation HITECH ont été intégrées dans HIPAA via la règle omnibus finale, ce qui a abouti à ce que les deux actes soient empilés sous une seule législation.
4. BYOD
Le Bring Your Own Device (BYOD) est une pratique conceptuelle où les employeurs de la santé autorisent le personnel médical à utiliser des appareils personnels tels que, mais sans s'y limiter, les smartphones et les tablettes pour des tâches officielles. Les choses pourraient se détériorer en un instant si votre solution mHealth n'est pas personnalisée pour les protocoles de sécurité BYOD. Par exemple, imaginez un scénario où un employé perd son smartphone avec l'appareil ayant accès à des informations de santé protégées (PHI) critiques.
C'est là qu'une stratégie de gestion des appareils mobiles bien pensée entre en jeu. À condition que les développeurs de l'application aient intégré une fonction d'effacement à distance dans la solution mHealth, vous pouvez effacer les données associées à l'appareil perdu. Des fonctionnalités similaires au sein du parapluie BYOD incluent la sécurisation des applications client telles que les e-mails et les navigateurs. Prendre note de ces détails lors des étapes initiales du SDLC pourrait éventuellement aider les startups à obtenir une approbation BYOD.
5. RGPD
Le règlement général sur la protection des données a été créé par l'Union européenne (UE) et s'applique aux applications pour smartphones qui collectent et traitent les données des clients des citoyens de l'Union européenne. Avec des discussions sur des itérations similaires de cette loi dans des travaux au-delà des frontières de l'UE, il est considéré comme une mesure de sécurité pour les développeurs d'applications de créer des solutions mHealth conformément à la même chose. La protection de la vie privée est l'essence même du RGPD à travers lequel les autorités fédérales ont tenté (avec succès) de confier une partie du contrôle des données personnelles au profane. Il maintient également les pratiques commerciales relatives à la gestion des données privées au grand jour.

Les dispositions du RGPD exigent que les applications mobiles demandent une autorisation, en d'autres termes le consentement actif de l'utilisateur , avant de collecter ou de traiter leurs données. L'application doit permettre à l'utilisateur de partager facilement son accord via une case à cocher ou tout autre bouton pour cliquer et enregistrer l'action. De plus, ces cases à cocher ne doivent pas être pré-cochées afin d'impacter psychologiquement le choix de l'utilisateur qui doit rester sans entrave. La page Termes & Conditions doit avoir son propre bouton "J'accepte". Le RGPD a largement démocratisé le contrôle des données personnelles car même après avoir donné leur consentement, si les utilisateurs le souhaitent, ils peuvent révoquer tous les droits accordés à l'application et se désengager. Activer une approbation GDPR des autorités serait relativement facile, à condition que les ingénieurs de la société de développement d'applications mobiles trouvent une solution compte tenu de cette discussion.
Dernières pensées
Les dépenses nationales de santé devraient atteindre 5,7 billions de dollars d'ici 2026 grâce aux technologies numériques telles que la santé mobile, la télémédecine, les capteurs, les technologies portables et les outils de surveillance à distance. Ces tendances en matière de soins de santé sont révélatrices d'une marche ascendante de solutions médicales jamais vues auparavant qui intègrent la technologie pour une sensibilisation instantanée du public. Ils sont également censés rendre les soins de santé abordables pour tous en tant que droit fondamental et non en tant que service à bénéficier. Pendant que vous vous concentrez sur le côté commercial de l'entreprise, laissez Appinventiv - l'une des principales agences de développement d'applications de santé aux États-Unis être en mode veille comme votre guide technologique.
Nous attendrions d'entendre vos pensées.
